從頭合成一個完整的單細胞生命,是當代生命科學面臨的一項重大挑戰。目前,科學家已在構建基礎生命功能模塊方面取得進展,例如在人工磷脂囊泡中實現DNA復制,以及利用前體分子合成磷脂以促進囊泡表面積的增長。然而,僅將這些功能模塊進行簡單組裝,尚難以實現生命活動的有序運行。當前面臨的主要瓶頸之一,在于對這些模塊之間協同工作的基本原理仍缺乏系統認識,這也限制了人工合成細胞形成生長、復制與分裂這一完整生命循環的能力。
針對這一關鍵問題,中國科學院深圳先進技術研究院合成生物學研究所劉陳立研究員團隊長期致力于探究天然細胞中DNA復制、生物量積累和細胞分裂等核心功能模塊的協同機制。在前期研究中,團隊以大腸桿菌為模型,利用定量合成生物學方法,揭示了細胞生長速率與細胞尺寸之間的數學規律,并發現了細菌通過“分裂許可物”來協同生長和分裂的新機制(Nature Microbiology 2020)。
在此基礎上,團隊進一步發揮定量合成生物學研究范式的優勢,設計合成了一套能夠實時監測DNA復制關鍵啟動蛋白DnaA活性的“分子探測器”,首次在活細胞中觀測到DnaA活性振蕩的峰值始終精準出現在DNA復制起始時刻,從而在實驗上直接驗證了經典理論中“DnaA活性決定DNA復制起始時機”的核心預測。此外,為解釋“DnaA表達停止后DNA仍可進行多輪復制”這一經典理論未能充分闡釋的現象,團隊通過結合數學建模與實驗驗證,創新性地提出了DnaA活性調控的“擠出”機制。該機制表明,可能存在某種調控蛋白能夠將結合在DNA上的DnaA“擠出”,使其重新獲得啟動DNA復制的活性。進一步研究提示,H-NS蛋白很可能在其中發揮關鍵調控作用。
該工作不僅首次直接證實了DnaA活性的周期性振蕩是觸發DNA復制的核心信號,還系統揭示了細菌通過“擠出”機制實現對DNA復制過程的精確時序調控,為理解生命體中DNA合成與生物量增長之間的協同機制提供了嶄新的理論視角。
相關成果于11月18日以"Extrusion-modulated DnaA activity oscillations coordinate DNA replication with biomass growth"為題,正式被eLife雜志收錄。
DNA復制起始是細菌細胞周期調控的關鍵節點。學界普遍認為,大腸桿菌通過精確控制DNA復制的起始時機,實現DNA的線性合成與生物量指數增長之間的協調匹配。經典理論指出,關鍵啟動蛋白DnaA的持續合成可以反應生物量的積累,其與DNA的相互作用則能感知DNA合成狀態,進而通過活性變化決定復制起始時機。然而,長期以來,領域內并未直接觀測到DnaA活性變化與DNA復制起始之間的動態關聯,且在DnaA合成被阻斷之后,DNA復制仍可啟動,這些現象無法用現有理論完整解釋,表明人們對細菌生長與DNA復制之間的協同機制認識尚不全面。
合成DnaA活性“探測器”:定量其振蕩與DNA復制起始的關系
為直接觀測DnaA蛋白活性的細胞周期性振蕩,劉陳立團隊構建了DnaA活性可定量調節的平臺菌株,設計并合成了一系列可響應DnaA活性的合成啟動子。通過系統定量這些啟動子對DnaA活性變化的響應特性,團隊篩選出了對DnaA活性高度敏感且響應特異的啟動子Psyn66。隨后,借助mRNA熒光原位雜交技術,并以不響應DnaA活性的組成型啟動子Pcon作為參照,解析出Psyn66報告的DnaA活性的細胞周期變化規律。定量分析表明:無論生長速率如何改變或基因表達受到何種干擾,DnaA活性均隨細胞大小呈現顯著振蕩,該振蕩與dnaA基因的轉錄無關,且其峰值始終精準出現在DNA復制起始的時刻。這一結果在實驗上直接驗證了經典理論關于“細菌DnaA活性決定DNA復制起始時機”的核心預測。
DnaA活性調控“擠出”機制的提出及例證
在驗證經典理論的基礎上,團隊進一步探究了“DnaA表達停止后DNA仍可進行多輪復制”這一經典理論未能解釋的現象,并提出了一種新的DnaA活性調控機制——“擠出模型”(extrusion model)。該模型推測,除了已知的調控途徑外,細胞內可能還存在一種可與DNA結合的“擠出因子”,它能夠通過構象變化或競爭性結合,促使結合在DNA上的DnaA蛋白釋放到細胞質中,從而使DnaA活性在其合成停止后仍可維持一段時間的上升,以啟動后續幾輪DNA復制。
通過系統篩選細胞內可與擬核結合的蛋白質,研究團隊發現高豐度DNA結合蛋白H-NS具備“擠出因子”的潛在特征,隨后合成并引入相關基因線路,穩定或瞬時提升H-NS的表達水平,結果觀察到DnaA活性迅速增強,且DNA復制起始時機相應提前。該實驗結果為H-NS可能作為“擠出因子”參與調控DnaA活性提供了直接證據,進一步支持了“擠出模型”的合理性。
該研究秉承“造物致知”的研究理念,通過對生命系統進行合成重構與定量表征,并結合理論建模與仿真分析,揭示了協調細胞生長和DNA合成的新機制:DnaA活性的“擠出式”調控。這一發現不僅深化了人們對細菌細胞周期調控的理解,也為人工合成生命功能模塊的協同調控提供了新的設計思路。未來,在組裝具有復雜功能的人工生命系統時,或許可以借鑒此類天然調控機制,使各個功能模塊像細菌細胞內的高度協同網絡一樣,實現有序、高效且穩定的動態運轉。相關研究得到了國家自然科學基金、中國科學院戰略性先導B科技專項等多個項目的支持。中國科學院深圳先進技術研究院合成所劉陳立研究員為該文章的通訊作者,助理研究員李登進、副研究員鄭海和白陽為該文章的共同第一作者。

圖1.?eLife雜志上刊發的文章截圖
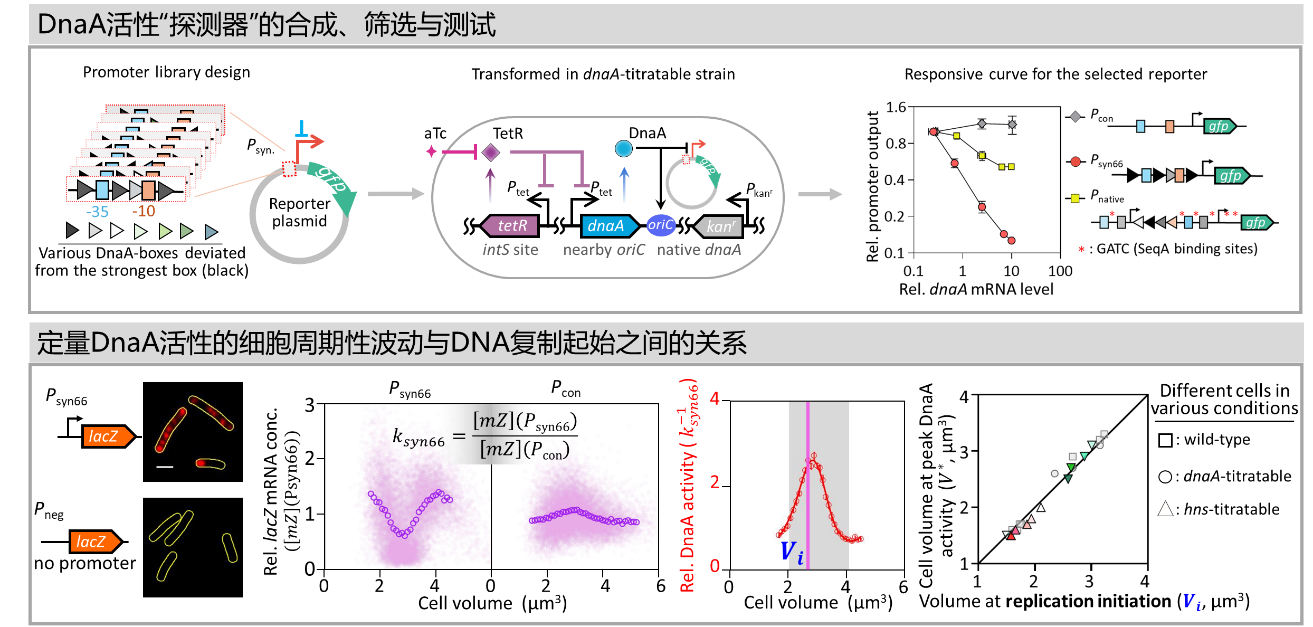
圖2.?合成DnaA活性“探測器”,定量其周期性振蕩與DNA復制起始的關系

圖3. DnaA活性調控“擠出”機制的提出及例證
附件下載:


