2025年11月,中國科學院深圳先進技術研究院醫學成像科學與技術系統全國重點實驗室張娜副研究員,開發出一套創新的深度學習框架,通過將“極坐標映射”這一數學變換引入人工智能分析系統,實現了對全腦及頸動脈血管壁的快速、精準、全自動分割。該技術通過將環形血管結構“展開”成平面進行分析,顯著提升了模型對薄層血管壁的識別能力。多中心臨床驗證表明,該系統性能卓越,為腦卒中風險的精準評估與防控提供了高效的量化新工具。研究以"Clinically Oriented Deep Learning Framework for Automated Vessel Wall Segmentation in Black-Blood MRI: A Multi-Center Study"為題,發表于國際影像學領域權威期刊European Radiology。
動脈粥樣硬化斑塊是導致缺血性腦卒中的重要原因。傳統的評估方法主要關注血管腔內的狹窄程度,往往難以有效識別那些雖未引起重度狹窄、卻具有高破裂風險的斑塊。與之不同,黑血MR血管壁成像技術能直接顯示血管壁的細微結構,清晰呈現斑塊的形態、分布及其強化特征,對于精準識別高風險斑塊、量化血管疾病負擔具有重要意義。然而,該技術的臨床應用長期面臨一項關鍵瓶頸:依賴影像科醫生在數百張圖像上進行耗時且繁瑣的手動勾畫,這一過程不僅效率低下,且存在明顯的觀察者間差異,限制了該技術在大規模篩查與長期隨訪中的應用推廣。因此,開發一套“精準、高效且具備跨中心一致性”的自動化量化工具,已成為推動血管壁成像技術邁向規模化臨床應用的迫切需求。
針對上述挑戰,研究團隊創新性地提出了一個融合深度學習與血管結構先驗信息的全自動血管壁分割框架。該框架聚焦于血管壁薄、呈環形、斑塊導致形態復雜以及邊界模糊等多個核心難點,在深度學習框架中系統性地引入極坐標映射模塊,構建了由 “極坐標映射—特征連續性建模—結構敏感損失函數” 組成的系統性解決方案,有效克服了傳統笛卡爾坐標系下卷積神經網絡難以精準捕捉血管徑向特征的局限。
具體而言,團隊借鑒數學中的極坐標概念,將圓形的血管橫截面如同展開一幅卷軸般轉換為平面矩形結構,這種“線性化”處理顯著增強了模型對血管壁徑向厚度變化與連續性的表征能力,從而在解剖結構復雜的區域實現了分割精度的大幅提升。此外,為解決極坐標變換可能帶來的角度端點不連續問題,研究者設計了特征共享填充策略,確保了血管壁在角度維度上的形態連貫性,進一步提升了模型對真實解剖結構的建模精度。最后,團隊還提出了專門的極坐標Dice損失函數,重點優化在圖像中占比小、卻極具臨床意義的血管壁區域,使模型在復雜背景中仍能保持優異的邊界識別能力。
為驗證該方法的有效性與泛化能力,研究團隊整合了來自五家醫療中心的多源臨床數據。在內部測試中,系統對血管外壁、管腔及血管壁區域的分割精度均超過94%。尤為重要的是,在另外四家中心的獨立外部測試集上,系統性能表現依然穩定可靠,證明了其強大的跨中心適應能力。為進一步確立方法的國際競爭力,團隊在公開的MICCAI 2021血管壁分割挑戰賽數據集上進行了測試,模型取得了當前最高的血管壁分割精度,結果處于國際領先水平。
本研究不僅技術上具有創新性,在臨床轉化與應用層面也展現出重要價值。通過梯度加權類激活映射技術,團隊可視化揭示了模型的決策依據,顯示其注意力始終聚焦于解剖學相關的血管壁邊界,增強了臨床醫生對AI輔助診斷結果的信任度。該系統的成功應用,有望將醫生從繁重的手工標注中解放出來,實現秒級自動化分析,顯著提升臨床工作效率;同時,其輸出結果具備高度客觀性與一致性,可為血管壁厚度、斑塊負荷等關鍵量化指標的計算提供穩定基礎,輔助醫生更早、更準地識別高風險患者,為腦卒中的個體化預防與干預提供可靠的影像學支持。
中國科學院深圳先進技術研究院博士后陶學桐為論文第一作者,中國科學院深圳先進技術研究院張娜副研究員為論文的通訊作者。該研究得到了國家重點研發計劃、廣東省磁共振成像與多模系統重點實驗室和廣東省腦血管病轉化醫學創新平臺等項目的資助。

圖1:文章上線截圖
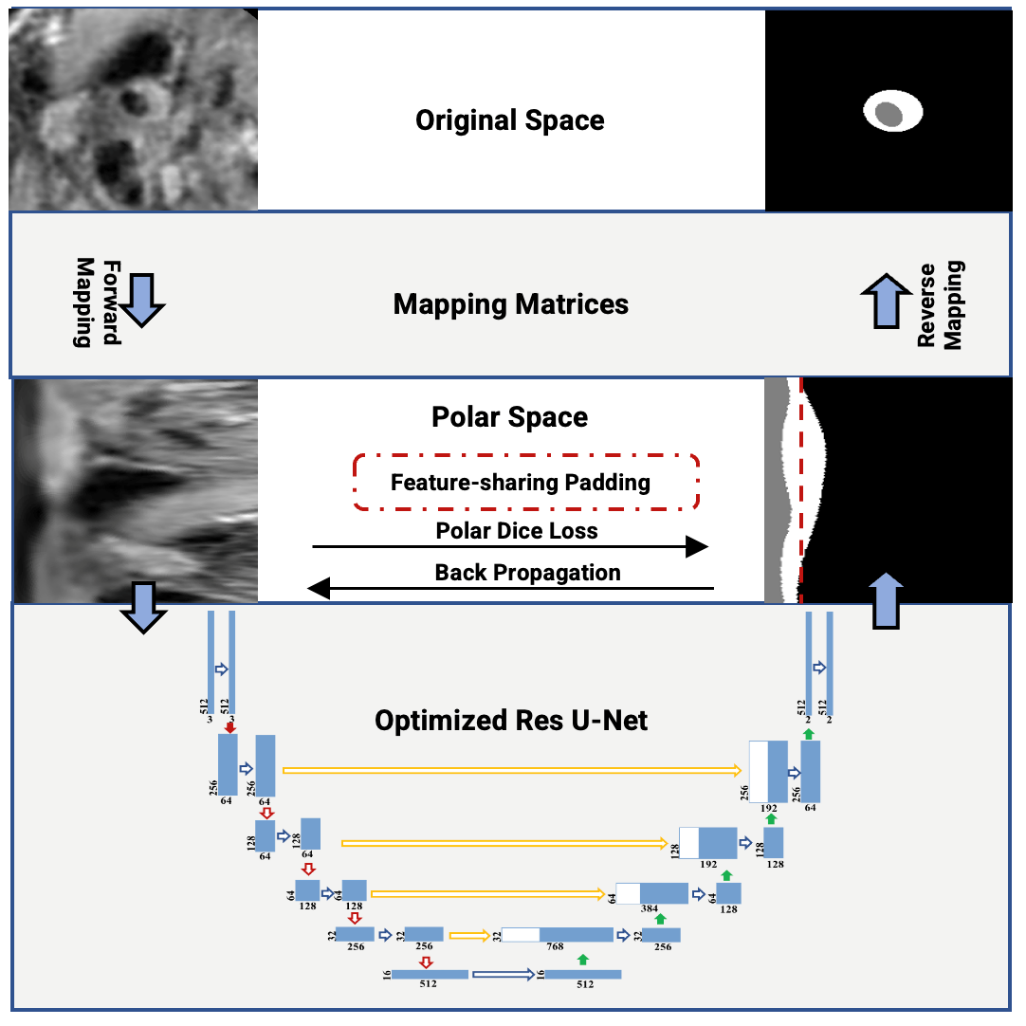
圖2:提出方法的總體技術路線圖
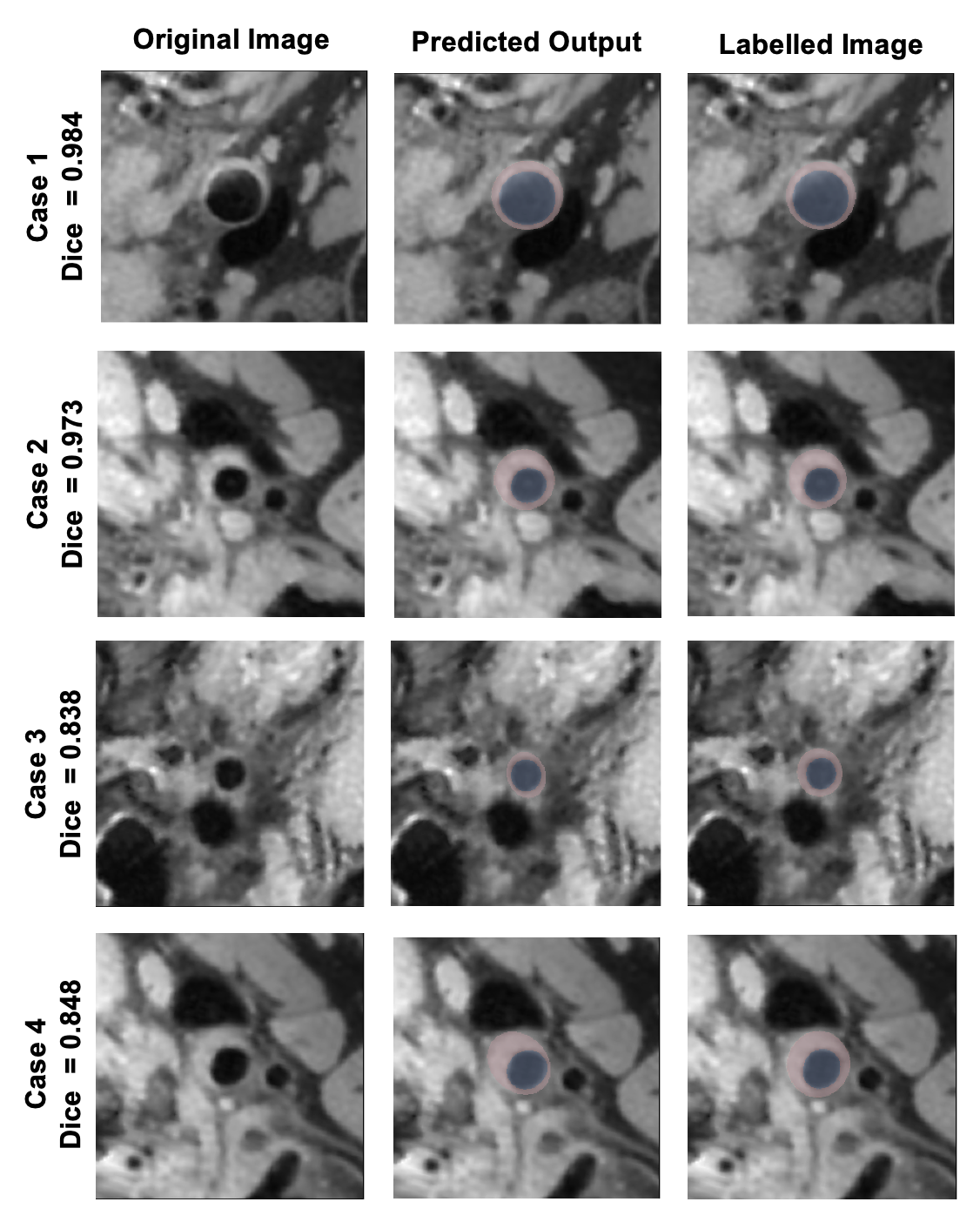
圖3:典型病例中自動分割結果與專家手工標注的一致性對比圖

圖4:模型在不同坐標域下的?Grad-CAM?可視化,用于展示其關注的關鍵區域
附件下載:


