人類腸道微生物組蘊藏著上千萬個基因,這些基因所編碼的蛋白質在人體的代謝、免疫等過程中發揮重要作用,也是開發疾病治療新技術的重要資源庫。然而,微生物蛋白質的進化多樣性,給基于序列同源的功能推斷方法帶來了挑戰。例如,在腸道噬菌體基因組中,有超過75%的蛋白無法注釋功能。此外,腸道細菌中廣泛存在宿主同工酶,但是這些酶與其真核同源基因蛋白的序列同源性很低,往往難以被識別。與序列相比,蛋白質的三維結構在進化中往往更為保守,這為解析腸道微生物的功能暗物質提供了新的研究思路——通過結構信息來推測蛋白質功能。腸道微生物的功能研究亟需從“序列檢索”走向“結構檢索”的新范式。
2025年11月26日,中國科學院深圳先進技術研究院定量合成生物學全國重點實驗室、合成生物學研究所(以下簡稱“深圳先進院合成所”)戴磊研究員課題組聯合北京大學汪鍇研究員、香港中文大學李煜教授的合作團隊在Cell Host & Microbe發表了題為"Exploring Functional Insights into the Human Gut Microbiome via the Structural Proteome"的研究論文。該研究建立了人體腸道微生物的蛋白質結構組數據庫和結構檢索方法,顯著提高了對噬菌體蛋白、菌源宿主同工酶等功能暗物質的預測能力大幅提高了噬菌體蛋白、菌源宿主同工酶的功能識別能力。基于這一方法,研究團隊成功驗證了腸道致病菌的噬菌體裂解酶,并首次揭示了腸道細菌的褪黑素合成途徑。
構建人體腸道微生物蛋白質結構組數據庫
首先,研究團隊構建了人體腸道微生物蛋白質結構組數據庫 (human Gut Microbial Protein Structure database,https://www.gmpsdb.cn/)。該數據庫涵蓋968個腸道細菌和1255個腸道噬菌體基因組所編碼的約270萬個蛋白結構(圖1)。
噬菌體蛋白的結構聚類與功能驗證
由于噬菌體基因組的快速進化,大部分噬菌體編碼的蛋白難以通過序列比對進行注釋。研究團隊采用結構比對和聚類方法,研究噬菌體蛋白的功能注釋和進化規律,發現許多噬菌體蛋白與已知功能蛋白之間存在結構相似度,可以大幅提高噬菌體蛋白的功能推斷能力(圖2)。
噬菌體裂解酶是一種噬菌體編碼的溶菌酶,能夠高效切割細菌細胞壁。通過系統分析噬菌體裂解酶的結構多樣性,研究團隊發現其存在結構域重排的進化機制。進而選取人體腸道致病菌噬菌體來源的裂解酶,通過合成生物學技術,成功驗證了其針對人體腸道致病菌的裂解活性(圖3)。此外,一部分噬菌體裂解酶具有很高的物種靶向性,有望成為微生物組精準編輯的平臺技術。
腸道菌源-宿主同工酶的結構檢索與功能驗證
研究團隊進一步將結構檢索的方法拓展至腸道菌源的宿主同工酶。前期研究發現,腸道細菌編碼的酶能模擬宿主酶的功能,參與疾病的發生發展過程。通過結構檢索,研究團隊在青春雙歧桿菌(Bifidobacterium adolescentis)、多形擬桿菌(Bacteroides dorei)中發現了參與褪黑素合成的關鍵酶,首次揭示了腸道微生物的褪黑素合成途徑(圖4)。
動物實驗表明,菌源酶能夠顯著調節宿主體內的褪黑素水平,進而影響腸道生理與疾病狀態(圖5)。
最后,研究團隊開發了人工智能方法Dense Enzyme Retrieval(DEER),能夠快速、高效識別同工酶,其性能顯著優于現有的基于序列或結構比對的方法(圖6)。DEER的模型訓練運用了融合結構信息的蛋白質語言模型及對比學習技術,實現了對酶功能的準確預測;DEER模型的推理運用了密集檢索技術,實現不依賴比對的快速檢索;DEER模型的框架不僅適用于遠源酶的挖掘,未來還可進一步拓展到其他功能的蛋白研究。
綜上所述,本研究提出蛋白結構檢索的微生物組功能研究范式,不僅建立了人體腸道微生物蛋白質結構組數據庫,還驗證了多種噬菌體裂解酶和菌源宿主同工酶的功能,為解析人體腸道微生物組的功能暗物質提供了重要的工具和思路。
深圳先進院合成所戴磊研究員是本研究的主要通訊作者,北京大學汪鍇研究員和香港中文大學李煜教授為共同通訊作者。深圳先進院合成所助理研究員劉紅賓博士是本研究的第一作者,深圳先進院合成所助理研究員沈俊濤博士、北京大學張志威博士、香港中文大學王久銘博士、深圳先進院合成所張成辛研究員為論文的共同第一作者。北京大學姜長濤教授、智峪裕生科王晟博士、深圳先進院合成所司同研究員和馬迎飛研究員對于本研究提供了重要支持。該項研究成果獲得國家重點研發計劃、國家自然科學基金等項目的資助。本研究獲得了深圳合成生物研究重大科技基礎設施和深圳合成生物學創新研究院公共技術平臺提供的支持。
戴磊課題組在定量生物學與合成生物學的交叉領域開展研究,致力于實現復雜微生物組在基因層次、群落層次的功能預測和精準編輯。近年來,以通訊作者(含共同) 在Cell Host & Microbe(2025,2023)、Nature Biomedical Engineering (in press)、 Nature Communications(2025,2024,2023)、The ISME Journal(2022)等期刊發表研究論文。課題組長期招收人工智能、合成生物學、微生物組學等相關專業博士后,聯系郵箱:lei.dai@siat.ac.cn。

原文鏈接:https://doi.org/10.1016/j.chom.2025.11.001

圖1.?人體腸道微生物的蛋白質結構組數據庫

圖2.?基于結構聚類的噬菌體蛋白功能推斷

圖3.?針對人體腸道致病菌的噬菌體裂解酶活性驗證
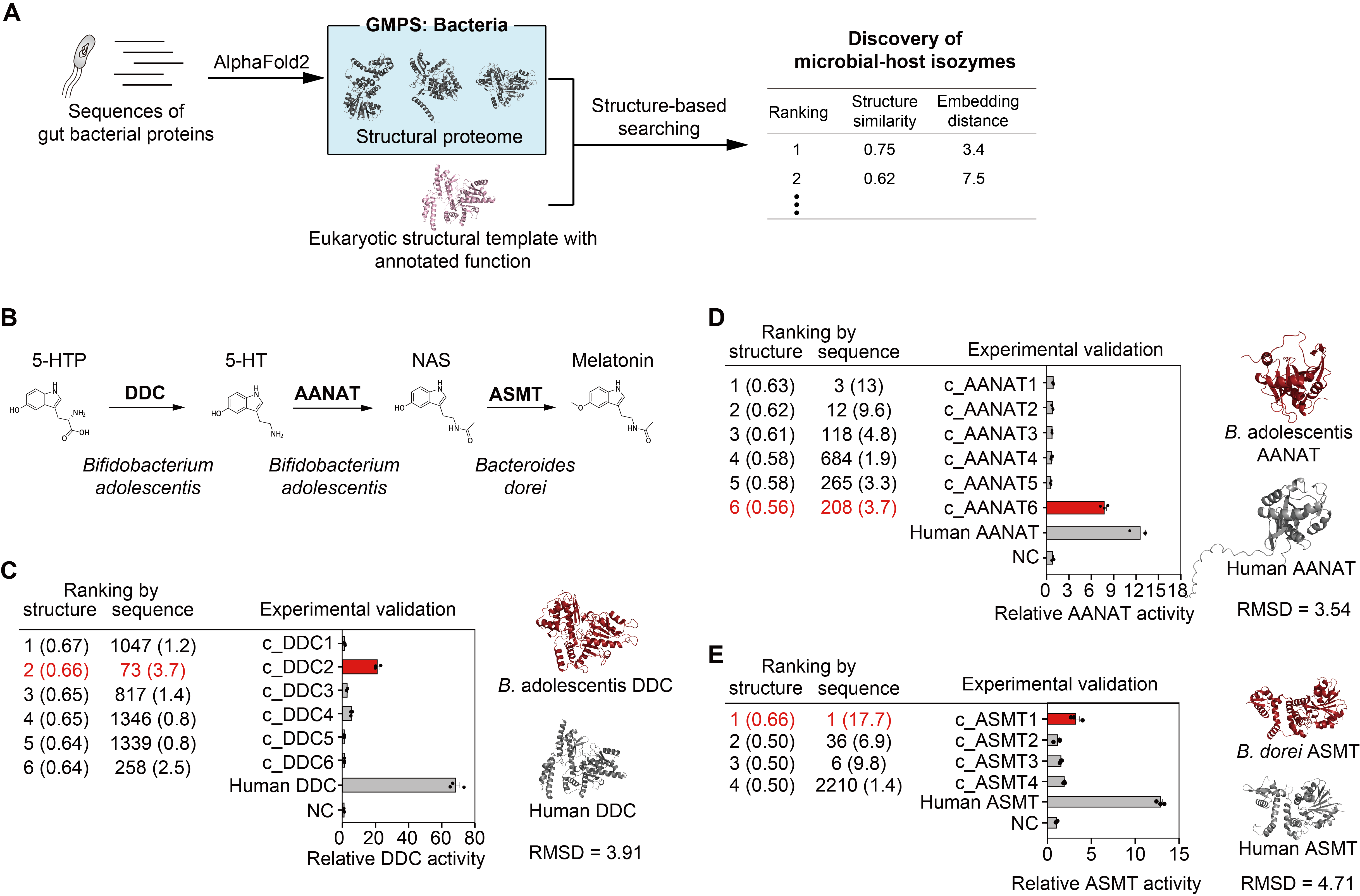
圖4.?基于結構檢索發現腸道菌的褪黑素合成酶

圖5.?菌源酶能夠顯著調節宿主體內的褪黑素水平

圖6.基于人工智能DEER的腸道菌源宿主同工酶挖掘
附件下載:


