




Nature Structural & Molecular Biology | 深理工(籌)葉克強團隊在阿爾茨海默癥發病機制研究領域獲得新進展
北京時間2022年3月25日,Nature Structural & Molecular Biology 雜志在線發表了深圳理工大學(籌,暫定名,以下簡稱“深理工”)葉克強團隊和武漢大學人民醫院張振濤團隊的最新成果。研究團隊發現腦內藍斑部位的去甲腎上腺素代謝產物DOPEGAL共價修飾Tau蛋白的K353位點,促進Tau的聚集和病變的播散。本研究為探索阿爾茨海默病(Alzheimer’s disease, AD)的發病機制提供了新的視角。

論文上線截圖
AD是臨床上最常見的神經退行性疾病,腦內Tau蛋白的異常聚集是AD重要的病理表現。但迄今為止,Tau蛋白異常聚集的分子機制尚不明確。病理學研究發現藍斑是腦內Tau蛋白聚集的起始位點之一,Tau蛋白首先在藍斑形成病理性聚集體,并向其它腦區播散,導致腦內廣泛的Tau蛋白聚集和神經損傷,最終導致認知功能障礙的發生。那么,為何藍斑部位的Tau蛋白更容易聚集呢?
研究團隊針對腦內Tau蛋白聚集的分子機制進行了長期的探索。團隊前期研究發現藍斑部位的單胺氧化酶A(MAO-A)將去甲腎上腺素氧化為DOPAGEL,DOPAGEL激活了天冬酰胺內肽酶(AEP)的表達,AEP剪切Tau蛋白,促進其聚集和播散(Journal of Clinical Investigation, 2020)。
接下來,該團隊發現ApoE3與Tau相結合,減少AEP對Tau的剪切,但AD相關的等位基因ApoE4失去了結合Tau蛋白的能力,使Tau更容易被AEP剪切。另一方面,ApoE4能夠抑制囊泡單胺轉運蛋白VMAT的水平,使去甲腎上腺素難以進入突觸囊泡,而滯留在胞漿中被MAO-A氧化,生成DOPAGEL(Acta Neuropathologica, 2021)。
在最新發表的研究中,該團隊進一步深入研究了DOPAGEL對Tau的修飾作用,發現DOPAGEL可以直接共價修飾Tau的K353位點,與全長的Tau相比,AEP剪切形成的Tau蛋白片段更容易被DOPAGEL修飾。DOPAGEL修飾的Tau蛋白聚集能力更強,而且形成的病理性聚集體作為“種子”誘導Tau蛋白單體的聚集能力更強。在Tau轉基因小鼠腦內阻斷MAO-A的活性,或者將Tau的K353位點突變后可以阻斷DOPAGEL對Tau的修飾,部分緩解Tau病變的播散。
本研究的意義在于揭示了AD發病過程中,為何藍斑區域的Tau蛋白首先發生聚集形成病理性包涵體,對理解AD患者腦內Tau蛋白聚集體的起始和播散過程具有非常重要的啟示作用。這樣在AD疾病的早期對MAO-A用小分子藥物進行抑制可能極大減緩Tau的病理改變。但是,這一新機制的發現是否也可以推廣到其他與Tau病理改變有關的Tauopathies疾病還需要進一步實驗驗證。
葉克強教授是深理工(籌)生命健康學院生物學系主任,曾任美國埃默里大學終身教授。他是世界公認的神經退行性疾病領域國際權威,尤其在小分子化合物靶向藥物治療神經退行性疾病方向取得了突破性進展,他所發現的多個藥物現已經或即將進入臨床試驗。葉教授目前正帶領團隊進行與衰老相關疾病新藥物的開發研究。此次發布的科研成果,也是其在阿爾茲海默癥機制研究領域取得的又一重要進展。
原文鏈接:https://www.nature.com/articles/s41594-022-00745-3
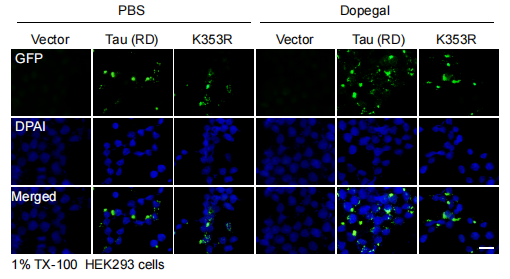
圖1:DOPAGEL促進細胞內Tau的聚集而K353R突變可以阻斷DOPEGAL的促進作用
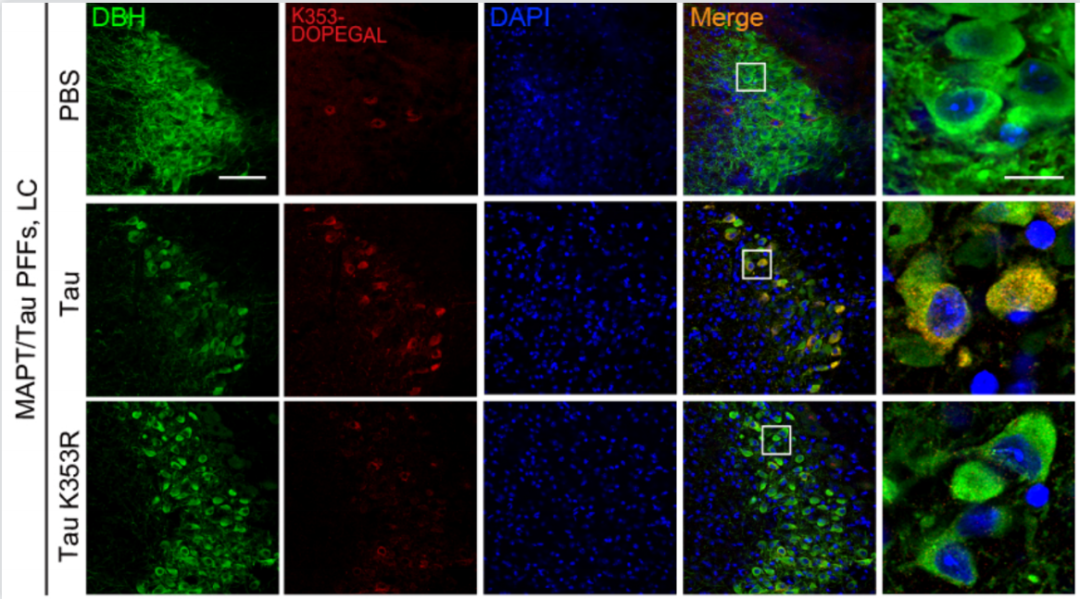
圖2:阻斷DOPEGAL對Tau的修飾可以延緩Tau的聚集,向過表達Tau的轉基因小鼠腦內注射Tau聚集體可以誘導腦內的Tau聚集,而突變K3533位點后阻斷了DOPEGAL對Tau的修飾,腦內Tau的聚集減少