




深圳先進院揭示調節NK細胞抗腫瘤功能的新型卡控點分子
9月15日,中國科學院深圳先進技術研究院合成所田志剛課題組的最新研究成果以TIPE2 is a checkpoint of natural killer cell maturation and antitumor immunity為題在線發表于Science Advances雜志。論文報道了TIPE2分子負調控NK細胞的功能成熟與抗腫瘤免疫應答,表明TIPE2是NK細胞的卡控點分子,提示靶向TIPE2可能促進基于NK細胞的腫瘤免疫治療策略。深圳先進院畢嘉成副研究員和中國科學技術大學孫昊昱副教授為該文的通訊作者,畢嘉成副研究員同時是該文的第一作者。
當前免疫治療的快速發展正在改變腫瘤的治療范式,然而,并不是所有的患者都能從免疫治療中受益。在應對實體腫瘤等情況下,免疫治療仍面臨有效性和安全性不足等問題。另一方面,在合成生物學理念與技術的影響與驅動下,當前的免疫治療研究正往以工程化操控為主要特征的“合成免疫學”新階段發展,旨在通過設計與構建新型合成免疫分子、合成免疫細胞等,對免疫應答進行理性操控,從而實現腫瘤等重大疾病的免疫治療。而 “卡控點分子/ Immune Checkpoints”(對免疫系統具有重要調節作用的分子)作為合成免疫分子/細胞設計的基本元件,對其進行深入研究不僅能揭示免疫應答的調控規律,而且能提供工程化設計合成免疫分子/細胞的理論依據。因而,“卡控點分子”研究是當前“合成免疫學”研究的關鍵切入點。
NK細胞(天然殺傷細胞,Natural Killer cells)是一種固有免疫細胞,通過殺傷靶細胞、誘導靶細胞凋亡或分泌細胞因子來發揮對腫瘤的免疫監視功能。大量研究早已顯示NK細胞不僅在控制血液系統腫瘤及腫瘤轉移中發揮關鍵作用,而且NK細胞在實體腫瘤中的浸潤水平也與患者的預后密切相關。NK細胞在當前的腫瘤免疫治療研究中具有重要的地位,因為NK細胞不僅能識別并殺傷HLA低表達等逃逸T細胞應答的腫瘤細胞類型,而且NK細胞對基于T細胞的免疫治療(如靶向PD-1/PD-L1的“卡控點療法”)也具有促進作用,此外NK細胞還天然具有作為“通用型”合成免疫細胞療法底盤細胞的優勢。盡管如此,NK細胞在腫瘤微環境中會受到一系列免疫抑制性細胞、分子等的負向調控,進入功能低下的“免疫耗竭”狀態(圖1);為了充分發揮基于NK細胞的免疫治療策略的優勢,我們需要深入揭示腫瘤相關NK細胞的功能調節機制。
課題組前期已發現表達在細胞表面的卡控點受體TIGIT(Hepatology 2014a,2014b; Nat Immunol 2018)和A3AR(Cell Mol Immunol 2021)在疾病狀態如腫瘤、組織損傷與再生等過程中對NK細胞的功能具有負調控作用。在上述研究基礎上,我們考慮到NK細胞在穩態條件下的成熟過程對于NK細胞最優功能水平的獲得至關重要,而我們對該過程中的負調控因子了解不多,為了進一步探索NK細胞的潛在卡控點分子,我們對正常狀態下人和小鼠外周NK細胞進行了單細胞轉錄組分析,結果顯示NK細胞在功能成熟過程中存在著對應NK細胞從“不成熟”到“成熟”分化過程的幾個亞群,我們同時發現,早前被報道具有介導免疫耐受功能的TIPE2分子伴隨著NK細胞的成熟而逐漸表達升高(圖2),呈現出與NK細胞成熟相關的表達特征。
我們通過NK細胞特異性缺失TIPE2的小鼠模型發現,NK細胞缺失TIPE2之后成熟亞群的水平升高、且NK細胞在群體水平和單個細胞水平均具有更強的效應功能(圖3),表明TIPE2負調控了NK細胞的功能成熟過程。而且,我們進一步通過腫瘤模型發現,NK細胞缺失TIPE2之后顯著抑制了腫瘤細胞在體內的生長,伴隨著腫瘤浸潤NK細胞水平的增加與功能分子表達水平的提高,從而表明TIPE2負調控NK細胞的抗腫瘤免疫應答(圖4)。因此,我們通過這項研究發現,TIPE2是負調控NK細胞功能成熟與抗腫瘤免疫應答的卡控點分子,靶向TIPE2可能促進基于NK細胞的抗腫瘤免疫治療策略。
該工作獲得了科技部國家重點研發計劃、國家自然科學基金、中國科學院定量工程生物學重點實驗室、深圳合成生物學創新研究院等項目的支持。
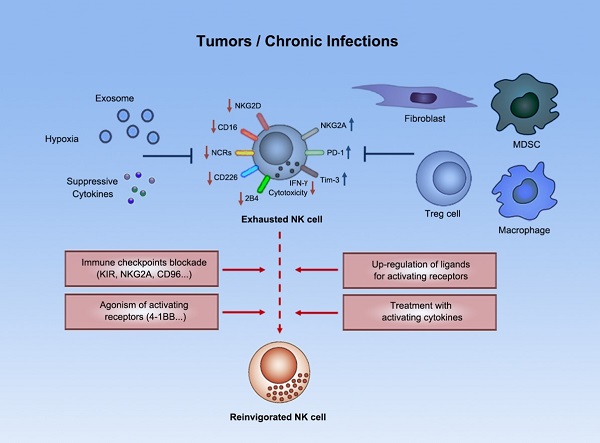
圖1. NK細胞在腫瘤微環境中進入功能低下的“免疫耗竭”狀態
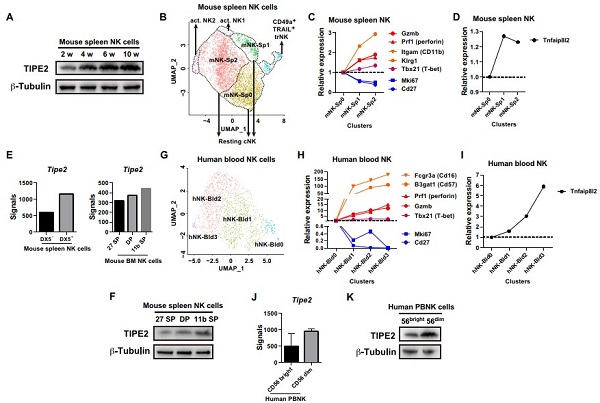
圖2. TIPE2的表達水平與NK細胞的功能成熟相關
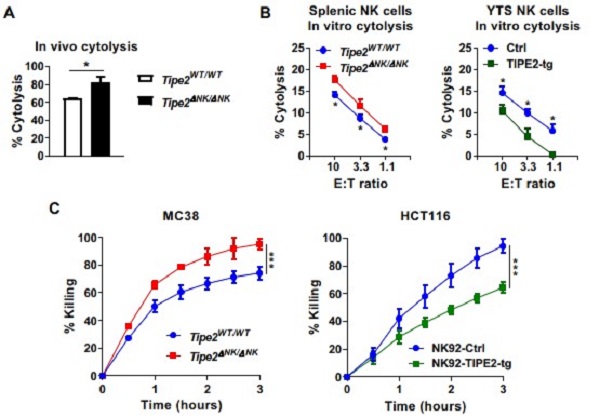
圖3. TIPE2負調控NK細胞的效應功能
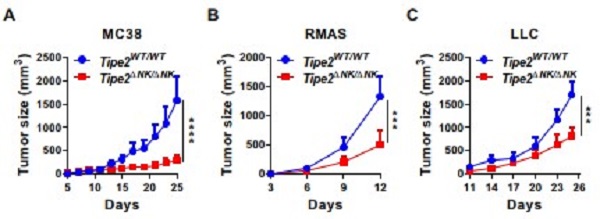
圖4. TIPE2負調控NK細胞的抗腫瘤免疫應答