




深圳先進院等在納米載藥系統(tǒng)治療骨髓炎領(lǐng)域獲得新進展
近日,中國科學(xué)院深圳先進技術(shù)研究院醫(yī)藥所人體組織與器官退行性研究中心王國成副研究員團隊與海軍軍醫(yī)大學(xué)第一附屬醫(yī)院許碩貴教授團隊,在納米載藥系統(tǒng)治療骨髓炎領(lǐng)域獲得新進展。相關(guān)研究成果以Silicon incorporation into hydroxyapatite nanocarrier counteracts the side effects of vancomycin for efficient chronic osteomyelitis treatment為題發(fā)表在化學(xué)工程與技術(shù)學(xué)科的權(quán)威刊物Chemical Engineering Journal(https://doi.org/10.1016/j.cej.2020.126821,影響因子10.652)上。本研究中深圳先進院助理研究員徐正江、海軍軍醫(yī)大學(xué)第一附屬醫(yī)院夏琰博士和周潘宇博士為并列第一作者。
慢性骨髓炎是指由細菌所引起的并伴有骨質(zhì)破壞的慢性炎癥過程,常繼發(fā)于急性骨髓炎,多由于開放性創(chuàng)傷、多次骨折手術(shù)或細菌血源性播散所引起,臨床表現(xiàn)為患肢局部破潰流膿、組織水腫、死骨形成以及寒戰(zhàn)、高熱、甚至感染性休克等全身癥狀,一直是臨床骨科醫(yī)生所面臨的最為棘手的問題之一。目前,臨床治療慢性骨髓炎的方法是通過手術(shù)徹底清除病灶(死骨和炎癥組織)并結(jié)合長達4至6周全身抗生素治療。但是長期全身大劑量使用抗生素的副作用多,可引起如耳毒癥、肝腎毒性、腸胃相關(guān)并發(fā)癥、影響骨骼發(fā)育等并發(fā)癥,且很難達到并維持骨髓炎感染部位所需的有效血藥濃度。
通過藥物載體實現(xiàn)抗生素局部遞送不僅可以避免全身抗生素治療帶來的副作用,且可實現(xiàn)抗生素在感染部位的持續(xù)高濃度釋放。然而局部高濃度的抗生素雖能有效地控制感染,但卻會對周圍組織產(chǎn)生明顯毒副作用,甚至干擾新骨形成。因此,理想的抗生素載體應(yīng)具有雙重功能,即能可控/持續(xù)釋放抗生素來消除感染,同時具有高骨誘導(dǎo)活性以促進骨再生。目前新抗生素載體的研發(fā)主要集中在優(yōu)化其載藥量和釋放特性,而在很大程度上忽視了“如何抵消高濃度抗生素對骨再生的負面影響”這一問題。
生物活性離子對骨再生的促進作用被廣泛證實,其中硅離子在血管再生和骨再生方面的作用尤為明顯。在前期工作中,王國成研究團隊開發(fā)了多種含Si的骨修復(fù)材料,均具有較好的生物活性(Biomaterials, 2020, 232, 119645; ACS Appl. Mater. Interfaces, 2015, 7, 23412; Biomaterials, 2013, 34, 13, 3184; Colloids and Surf. B, 2019, 176, 420)。基于此,團隊提出如下假設(shè):生物活性Si離子有可能在抵抗抗生素的負面作用方面具有一定效果。
為了驗證本假說,本研究采用原位包裹法將一定厚度的介孔生物活性玻璃(MBG)包裹到納米羥基磷灰石(HAp)載體表面,通過負載抗生素(萬古霉素)構(gòu)建了含Si的納米藥物遞送系統(tǒng)。研究證明較單純的納米HAp而言,MBG的引入可提高藥物裝載量并優(yōu)化其緩釋功能。體外細胞實驗結(jié)果證明,MBG包裹納米載藥系統(tǒng)較HAp載藥組能夠更好地促進成骨細胞增殖和成骨分化。慢性骨髓炎動物模型實驗結(jié)果證明較單純的HAp載藥組,MBG包裹的載藥系統(tǒng)可以抑制感染,同時因Si離子的引入能減少萬古霉素對細胞的副作用,從而顯著提高感染部位的骨再生能力。團隊通過在含有萬古霉素的培養(yǎng)基中加入Si離子進行細胞培養(yǎng)實驗,進一步證實了Si離子可緩解萬古霉素對成骨細胞造成的負面作用。目前,研究團隊針對相關(guān)的分子機制展開研究。
該項目獲得國家重點研發(fā)計劃、國家自然基金、廣東省科學(xué)技術(shù)計劃、深圳市科技研究基金和上海市青年科技英才揚帆計劃等項目資助。
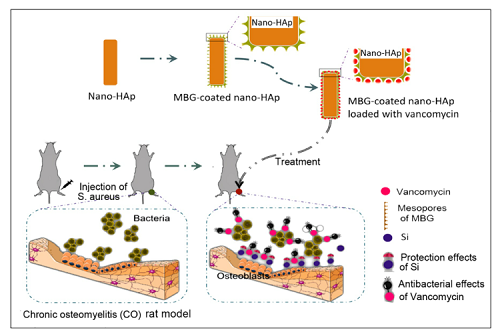
介孔生物活性玻璃包裹納米羥基磷灰石負載萬古霉素治療慢性骨髓炎的示意圖
