近年來隨著微塑料在人體中被檢測到的證據越來越多,微塑料的健康風險也備受關注。然而已報道的相關研究多聚焦于微塑料原始狀態的健康風險,或是致力于模擬微塑料在環境介質中的老化過程及其環境老化后的毒理學效應。對微塑料進入機體后長期滯留引發的“生物老化”特征及其毒理學效應仍缺乏系統認識。
12月30日,中國科學院深圳先進技術研究院李洋研究員團隊在Environmental Science & Technology發表研究論文,系統分析了微塑料在體內長期滯留過程中的“生物老化”理化表征變化,闡明生物老化過程能夠增強微塑料與關鍵炎癥信號分子相互作用,賦予微塑料“特洛伊木馬”功能,進而激活非典型炎癥信號通路,放大炎癥反應,最終加重機體炎癥病理。該研究為闡明微塑料體內長期命運與其健康風險機制之間的內在聯系提供了重要證據。
以往關于微塑料老化的認知,主要集中于其在自然環境中所經歷的光氧化、熱降解等過程,即“環境老化”。然而,當微塑料通過攝入等途徑進入人體后,由于其穩定的化學性質,難以被生物降解,部分可能長期滯留于組織內。在體內生理環境下,微塑料可能經歷持續數年的“生物老化”過程。然而生物老化對微塑料顆粒性質的影響,以及生物老化微塑料所引發的生物學效應,長期以來一直是一個尚未揭示的科學黑箱。另一方面,現有毒理學研究較多關注微塑料浸出液或其負載重金屬等化學物質后的毒性,卻忽視了微塑料與胃腸道等復雜生理環境中豐富的生物活性分子之間可能發生的特異性相互作用。值得注意的是,此類相互作用恰恰可能主導微塑料的長期健康風險。在腸腔及炎癥相關微環境中,脂多糖(LPS)作為革蘭氏陰性菌細胞外膜的關鍵成分,屬于病原體相關分子模式(PAMP),在腸屏障受損或菌群失衡等情況下更容易觸發宿主的炎癥反應。因此,探究生物老化微塑料與LPS的相互作用具有明確的生理學意義。
基于此,本研究旨在系統探究微塑料在體內生理環境中的長期生物老化效應。研究團隊利用在胃腸模擬液環境中生物老化12個月的聚苯乙烯微塑料,首次直接觀察并檢測其生物老化過程中的理化表征變化。結果顯示,長期體內環境暴露會深刻重塑微塑料表面,使其發生氧化、親水性增強,尤其是表面粗糙度顯著提升。這些界面理化性質的改變,預示著其與生物分子相互作用能力可能發生根本性變化。為精確量化生物老化微塑料與LPS的相互作用,本研究基于生物力學檢測,聯合原子力顯微鏡、分子動力學模擬及生物層干涉技術等多種手段證實,生物老化后增加的表面粗糙度,顯著增加微塑料與LPS之間的結合力。并且這種增強效果使老化微塑料能夠更大量且穩定地吸附LPS,在其表面形成更厚且致密的“LPS冠層”,使其從惰性顆粒轉變為搭載促炎分子的“特洛伊木馬”。當這些負載厚重LPS冠的老化微塑料被巨噬細胞識別并攝取后,微塑料載體可將LPS遞送至細胞質內部。這一過程使得LPS繞過了傳統細胞膜Toll樣受體4介導的識別路徑,在胞內直接被炎癥蛋白酶caspase-11識別,進而激活非經典炎癥小體通路:切割激活Gasdermin D并在細胞膜上形成孔道導致細胞焦亡;協同激活經典NLRP3炎癥小體,促進caspase-1對白細胞介素-1β前體的切割與成熟,成熟IL-1β經Gasdermin D孔道大量釋放到細胞外,最終放大炎癥反應。
進一步,研究團隊選取葡聚糖硫酸鈉(DSS)誘導的小鼠結腸炎模型,對生物老化微塑料負載LPS所產生的“特洛伊木馬效應”及其在腸道炎癥中的影響進行了檢測。結果顯示,口服負載LPS的生物老化微塑料顯著加劇了疾病嚴重程度,表現為更明顯的體重下降、結腸長度縮短及腸道屏障損傷加重。這些結果進一步證實,生物老化微塑料作為一種相對惰性的載體,可在腸道中吸附并攜帶LPS等強促炎因子。當負載LPS的生物老化微塑料被巨噬細胞攝取后,可將原本不易進入細胞的毒素“搭載”至胞內,從而增強細胞內炎癥信號的激活與放大,最終加劇炎癥反應并阻礙組織修復。
本研究首次完整揭示了微塑料在生理環境中的長期生物老化過程,及其對顆粒界面性質與炎癥信號傳遞能力的重塑作用。生物老化改變了微塑料的表面特性,使其從相對“惰性顆粒”轉變為能夠“攜帶并遞送促炎信號”的載體。載體被巨噬細胞攝取后,可將表面結合的促炎分子轉移至細胞內部,從而在細胞內觸發并放大免疫反應,最終加劇炎癥并擴展組織損傷。
本研究從環境毒理學角度闡明:顆粒物的健康風險并非僅由其初始理化性質決定。進入生物體后,顆粒經歷“生物老化”后,經過表界面性質重塑,與生理環境中的生物分子互作后,被賦予新的功能。在此過程中,一些原本低毒或無毒的微塑料,因獲得攜帶促炎分子、增強細胞內信號傳遞的能力,轉變為具有更高生物危害的“載毒復合體”,產生“特洛伊木馬效應”。
本研究通訊作者為中國科學院深圳先進技術研究院(SIAT)李洋研究員,張國芳副研究員,河北科技大學王英澤教授,河北師范大學常彥忠教授。巴塞羅那自治大學-SIAT聯培博士生李奇,SIAT王曉峰工程師,河北師范大學-SIAT聯培已畢業碩士徐雅晴為共同第一作者。研究工作得到了科技部重點研發計劃、國家自然科學基金、廣東省自然科學基金等項目的資助,并得到了西班牙?加泰羅尼亞納米科學與納米技術研究所Victor F. Puntes教授團隊的幫助。
本研究從微塑料—生物分子互作出發,闡明生物老化能夠增加微塑料的表面粗糙程度,改變其表界面性質,從而增強其與生物分子互作,最終揭示其免疫毒理學效應的分子機制。李洋研究員團隊長期圍繞納米顆粒與生物分子相互作用開展系統研究,致力于解析納米-生物分子互作規律及機制解析,闡明納米顆粒生物學效應的分子機制,為評估納米顆粒的毒理學效應機制或開發納米分子靶向藥物,提供全新的理論基礎和研究范式。相關研究發表于Nature Nanotechnology,Journal of the American Chemical Society,Advanced Functional Materials等期刊。

原文鏈接:https://pubs.acs.org/doi/10.1021/acs.est.5c12882
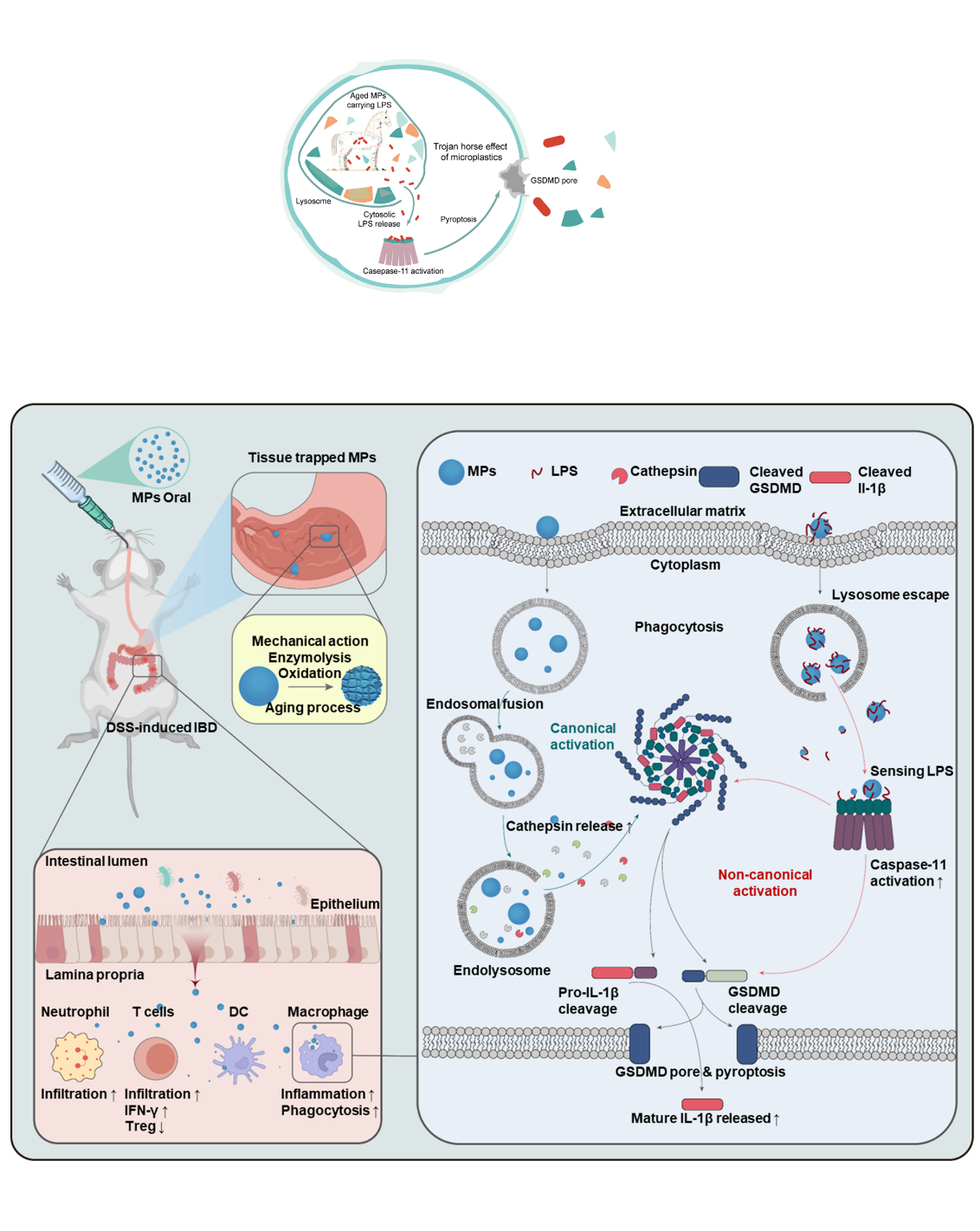
圖1.?生物老化微塑料攜帶脂多糖進入巨噬細胞并放大炎癥反應的“特洛伊木馬效應”機制
附件下載:


