膠質母細胞瘤(Glioblastoma,GBM)是成人中最常見且侵襲性最強的原發性腦腫瘤之一,患者預后極差,中位總生存期通常不足兩年[1][2]。替莫唑胺(Temozolomide,TMZ)是目前唯一被廣泛應用的一線化療藥物,可在一定程度上延長患者生存,但約90%的初始敏感病例最終會因獲得性耐藥而導致腫瘤復發[3]。如何有效克服TMZ耐藥仍是臨床治療中的重大挑戰。
1月9日,中山大學中山醫學院趙蔚教授與中國科學院深圳先進技術研究院/醫學成像科學與技術系統全國重點實驗室研究員董鵬團隊合作在Nature Chemical Biology發表了題為“Deacetylase-Independent HDAC1 Condensation Defines Temozolomide Response in Glioblastoma”的研究論文。該研究發現,替莫唑胺(TMZ)治療可誘導膠質母細胞瘤(GBM)細胞形成HDAC1-CTCF凝聚體,從而導致染色質結構重塑和DNA修復活性增強,促進TMZ獲得性耐藥的發生。更為重要的是,研究團隊鑒定出小分子化合物Resminostat能夠特異性靶向該凝聚體,在耐藥GBM的患者來源異種移植(PDX)模型中顯著恢復TMZ敏感性,有效克服腫瘤耐藥。
研究團隊首先利用董鵬教授自主研發的高通量三維超分辨成像技術3D-ATAC-STORM,發現TMZ耐藥GBM細胞的染色質可及性顯著降低,并系統描繪了其三維基因組結構特征。進一步的機制研究表明,耐藥細胞染色質可及性降低主要歸因于TMZ處理誘導HDAC1-CTCF凝聚體的形成,該凝聚體在染色質上聚集并限制局部開放性。
為探索藥物干預策略,研究團隊建立了針對HDAC1-CTCF凝聚體的高內涵篩選體系,發現小分子化合物Resminostat能夠特異性破壞該凝聚體的形成。在TMZ耐藥GBM的PDX模型中,Resminostat顯著逆轉腫瘤對TMZ的耐藥性,促進DNA損傷反應并抑制腫瘤進展。
進一步的機制研究表明,Resminostat對HDAC1-CTCF凝聚體的作用并不依賴于抑制HDAC1的經典組蛋白去乙酰化酶活性,而是通過干擾其固有無序區域(Intrinsically Disordered Region, IDR)介導的相分離過程實現。Resminostat可破壞 HDAC1-CTCF 凝聚體的形成與穩定性,從而抑制其介導的DNA修復復合物在損傷位點的組裝,降低DNA損傷修復效率并增強TMZ誘導的DNA損傷積累,最終有效克服腫瘤細胞的耐藥性。
本研究系統揭示了HDAC1-CTCF凝聚體介導的染色質重塑與DNA修復在膠質母細胞瘤替莫唑胺耐藥中的關鍵作用機制,拓展了對HDAC1生物學作用模式的理解。該研究證實小分子化合物Resminostat可通過破壞HDAC1-CTCF凝聚體從而恢復TMZ敏感性,為靶向腫瘤凝聚體以克服腫瘤耐藥提供了新的理論依據。
值得強調的是,Resminostat 已在皮膚 T 細胞淋巴瘤(ClinicalTrials ID: NCT02953301)、肝細胞癌(NCT02400788)及霍奇金淋巴瘤(NCT01037478)等多種腫瘤中開展過早期臨床研究,相關結果顯示,其安全性特征較為明確,整體耐受性處于可管理范圍內。雖然其在GBM中用于克服TMZ耐藥的療效尚未開展臨床驗證,但本研究為其轉化應用提供了堅實的理論與實驗基礎。未來研究可進一步優化Resminostat的血腦屏障通透性與腦內藥代動力學特征,以期實現其在GBM中的精準遞送與有效治療。
本研究由中山大學中山醫學院、中國科學院深圳先進技術研究院、南方科技大學、廣東省人民醫院及中南大學湘雅醫院等單位聯合完成。中山大學張欽凱博士、邱茹博士與南方醫科大學魯冰教授為論文共同第一作者;趙蔚教授與董鵬研究員為共同通訊作者;南方科技大學李依明教授和博士后方珂、石偉,以及中國科學院深圳先進技術研究院助理研究員朱虹霓,原研究助理王金泓為本研究的3D-ATAC-STORM成像做出了重要貢獻;中南大學湘雅醫院劉慶教授、龍文勇醫生及黃蒙醫生為本研究提供了重要的GBM臨床樣本與臨床數據支持。本研究得到了國家自然科學基金和深圳市醫學專項研究基金的支持。

圖1.?論文截圖
原文鏈接:https://www.nature.com/articles/s41589-025-02123-8
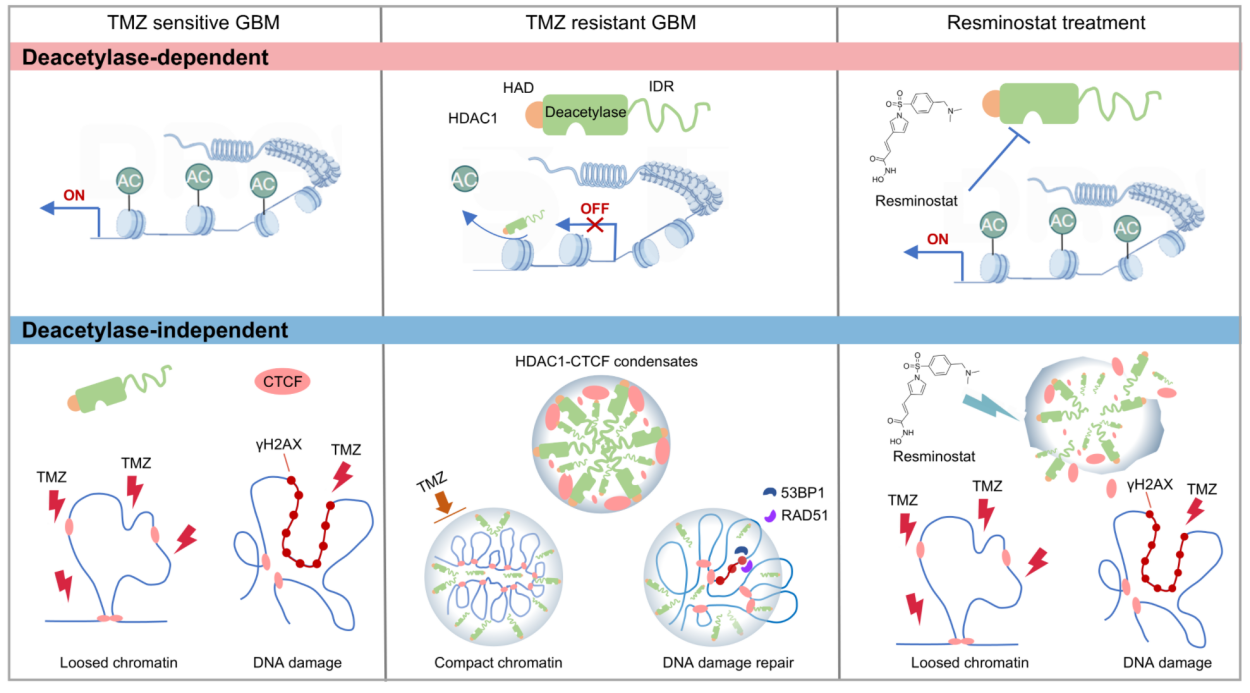
圖2.?替莫唑胺治療誘導膠質母細胞瘤產生耐藥性以及Resminostat克服耐藥性的分子機制。
附件下載:


