近日,中國科學院廣州生物醫藥與健康研究院腫瘤免疫研究組與香港大學萬鈞教授團隊在肝細胞癌(HCC)分子機制與靶向治療研究方面取得重要進展。團隊發現轉錄因子RELA在攜帶TP53R249S突變的HCC中發揮著關鍵抑癌基因作用,并進一步證實RELA激動劑白樺脂酸具有顯著的抗腫瘤效應,為該類預后不良的肝癌患者提供了新的潛在治療策略。相關研究成果以“RELA Ablation Contributes to Progression of Hepatocellular Carcinoma with TP53R249S?Mutation and is a Potential Therapeutic Target”為題發表在《Advanced Science》期刊上。
肝細胞癌是一種常見且高死亡率的惡性腫瘤,其治療仍面臨巨大挑戰。TP53是HCC中最常突變的腫瘤抑制基因,尤其在黃曲霉毒素暴露高發地區,超過90%的HCC病例中存在TP53R249S的特征性突變。然而,TP53突變驅動HCC發生發展的核心機制尚未完全闡明,這嚴重制約了針對性治療策略的研發。
為系統揭示人類HCC中的抑癌基因,研究團隊基于CRISPR/Cas9技術,對過表達MYC和TP53R249S的原代人肝細胞(MT-PHHs)進行了異種移植全基因組篩選。篩選結果顯示,RELA是其中最重要的候選抑癌基因之一。機制研究表明,在TP53R249S的基因背景下,RELA的缺失會上調細胞周期和干細胞特性相關基因,并促進上皮間質轉化(EMT),最終驅動原代人肝細胞在小鼠模型中原位轉化為HCC并促進其轉移。臨床上,RELA 低表達與肝細胞癌患者預后不良和腫瘤體積較大呈正相關。在分子機制層面,RELA表達降低會促進DVL1的表達,進而增強β-catenin的核轉位,最終激活致癌的Wnt/β-catenin信號通路。這一發現在HCC中明確了NF-κB與Wnt在腫瘤進展中的功能性協同關系,為理解HCC發病機制提供了新視角。此外,RELA的特異性激動劑——天然產物白樺脂酸(BetA)能夠有效增強RELA活性,并在異種移植瘤模型中顯著抑制攜帶TP53R249S突變的肝癌細胞的生長與轉移。這預示著白樺脂酸或其衍生物有望成為治療TP53R249S突變型HCC的潛在候選藥物。
RELA(亦稱p65)作為NF-κB信號傳導的關鍵轉錄因子,以往研究多報道其在多種癌癥中的促癌作用。本研究創新性地揭示了其在TP53R249S突變型HCC中作為抑癌基因的雙面功能,不僅深化了對RELA上下文依賴性功能的理解,也為該肝癌亞型的精準治療提供了理論依據和潛在靶點。
廣州健康院博士后吳質平、香港大學王喆和香港創新研究院再生醫學與健康創新中心鄭迪威博士為本論文的共同第一作者,廣州健康院李鵬研究員和香港大學萬鈞教授為共同通訊作者。該項目得到了國家重點研發計劃、國家自然科學基金面上項目、廣東省“一帶一路”聯合實驗室基金及GIBH自主部署項目等多個項目支持。
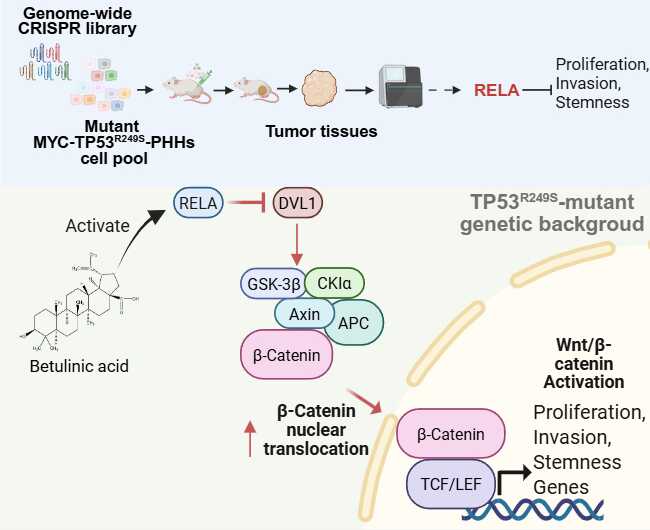
圖 1通過全基因組文庫敲除篩選RELA為HCC的新抑癌基因,RELA通過調控DVL1調節Wnt/β-catenin信號通路發揮抑癌功能,并可作為TP53R249S突變型肝癌治療的新靶點。
附件下載:


