基因劑量的變化在胚胎發育、疾病發生以及細胞命運決定過程中發揮著關鍵作用,其系統化解析對于精準理解生命過程至關重要。作為研究基因功能的核心策略,基因擾動近年來與單細胞組學的結合,使研究者能夠在全基因組尺度上系統解析基因的功能,并為虛擬細胞等人工智能模型的構建提供了寶貴的數據支撐。然而,現有的大規模基因擾動技術大多將基因功能簡化為“開/關”的二元模式,難以捕捉劑量依賴的連續效應。這種局限不僅削弱了對基因功能的全面理解,也可能在復雜生物學問題中引入不全面甚至錯誤的結論。
2025年10月3日,中國科學院深圳先進技術研究院合成生物學研究所陳萬澤課題組與瑞士洛桑聯邦理工學院(EPFL)Bart Deplancke課題組合作,在Nature Genetics發表了題為"Dissecting the impact of transcription factor dose on cell reprogramming heterogeneity using scTF-seq"的研究成果。團隊開發了scTF-seq技術,實現了劑量敏感的大規模基因擾動單細胞組學,并以轉錄因子介導的細胞重編程為模型,系統揭示了基因劑量在細胞命運調控中未被充分認識的多層次、非線性復雜效應。
為什么scTF-seq可以實現大劑量范圍的基因擾動并定量?
巧妙利用Tet-on啟動子內在噪音和逆轉錄病毒基因組不同整合位置表達活性差異,進一步結合高滴度病毒轉導的拷貝數差異(有別于傳統大規模擾動中常用的低滴度方式)。這種設計使得即使單一Doxycycline濃度下,轉基因的劑量也可以達到平均60倍,最高1000倍的極寬劑量分布。并結合3’scRNA-seq兼容的條形碼,定量解析轉錄因子劑量與轉錄組變化之間的對應關系,從而首次在大規模基因擾動背景下實現了“劑量敏感”的功能解析。
單基因的復雜非線性效應
scTF-seq揭示了轉錄因子劑量并非簡單線性地影響細胞命運。例如,KLF4在不同劑量下分別驅動與骨骼形成、細胞結構組裝或上皮發育相關的不同基因表達模式,表現出高度非線性的調控特征。這些復雜劑量效應為解釋細胞重編程的異質性提供了重要線索。
基因與其他細胞過程的互作
研究還發現,基因劑量效應與細胞周期等其他細胞過程密切相關。CEBPA和PPARG在高劑量下促進細胞周期退出并推動脂肪分化,而MYCN則突破常規,在細胞持續增殖的同時驅動分化,但最終伴隨細胞死亡。這揭示了基因劑量、細胞周期與分化過程之間的精細耦合關系。
多基因互作的劑量敏感性
在組合擾動實驗中,研究者發現不同轉錄因子的相互作用不僅取決于基因組合本身,還強烈依賴于基因劑量。同一對轉錄因子組合在不同劑量下可表現為可逆轉的協同或拮抗作用,且這種效應具有基因特異性,進一步凸顯了基因網絡調控的復雜性。
綜上,該研究表明,基因劑量不僅決定單個基因的功能,還塑造了基因與細胞過程的互作格局,以及多基因間的協同與競爭關系。scTF-seq為系統性地解析這些劑量依賴效應提供了新方法,產生的基因定量擾動數據也為精準細胞工程和虛擬細胞模型構建提供了關鍵支撐。
該工作由中國科學院深圳先進技術研究院合成生物學研究所和瑞士洛桑聯邦理工學院(EPFL)合作完成,陳萬澤研究員和Bart Deplancke教授為共同通訊作者,劉王杰(博士生)、Wouter Saelens(博士后)和Pernille Rainer(博士生)為共同第一作者。該工作獲得了重點研發計劃、國家自然科學基金委、深圳市醫學研究專項和深圳合成生物學創新研究院等項目的支持。
陳萬澤博士現為中國科學院深圳先進技術研究院合成生物學研究所研究員,博士生導師,主要研究方向是通過新技術的開發,理解細胞命運決定機制并進行改造和干預,得到國家自然科學基金優秀青年項目,國家重點研發計劃課題等重要項目的支持,相關成果以通訊和第一作者身份在Nature,Nature Genetics,Nature Cell Biology等期刊發表,被Nature Biotechnology,Nature Methods,Nature Immunology等多個雜志專文評述和高亮報道。歡迎感興趣的博士后、博士生和研究助理加入!

文章上線截圖,原文鏈接:https://www.nature.com/articles/s41588-025-02343-7
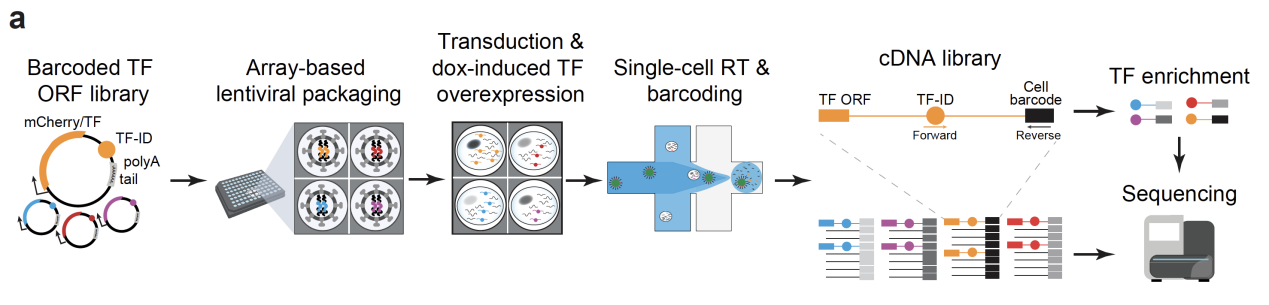
圖1:scTF-seq的原理圖示
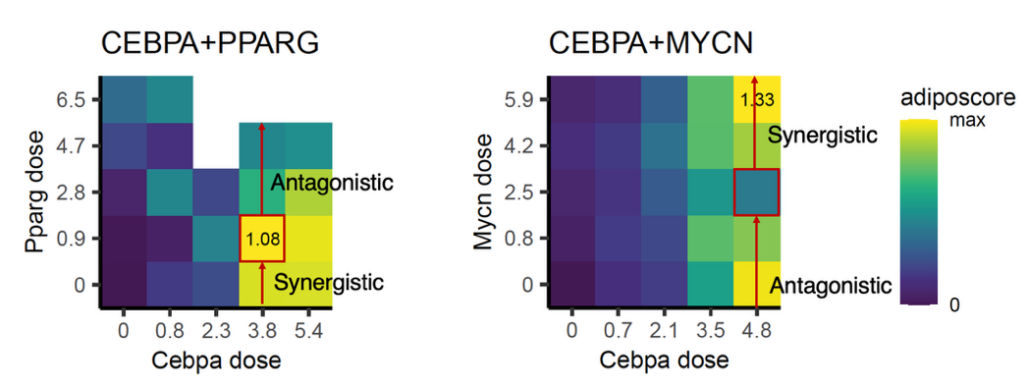
圖2:?兩個轉錄因子之間協同-拮抗效應的劑量可逆性
附件下載:


