靶向蛋白降解未配對(duì)的括號(hào)或引號(hào)!Targeted Protein Degradation,TPD)作為一種新的藥物研發(fā)策略,巧妙地利用了細(xì)胞自身的降解機(jī)制,實(shí)現(xiàn)對(duì)特定蛋白質(zhì)的選擇性清除。這一技術(shù)在解決傳統(tǒng)藥物難以觸及的“不可成藥靶點(diǎn)”問題上,展現(xiàn)了巨大潛力和前景。
位于細(xì)胞表面的細(xì)胞膜蛋白,廣泛參與細(xì)胞識(shí)別、物質(zhì)運(yùn)輸、信號(hào)轉(zhuǎn)導(dǎo)等生命活動(dòng),是重要的藥物研發(fā)靶點(diǎn)。近年來,針對(duì)細(xì)胞膜蛋白,涌現(xiàn)出了以LYTAC和AbTAC為代表的一系列靶向降解技術(shù)。這些技術(shù)的基本原理是構(gòu)建雙功能分子,實(shí)現(xiàn)靶蛋白與細(xì)胞膜表面溶酶體穿梭受體或E3連接酶之間的物理綁定,并借助這些受體或酶的生物學(xué)活性,促進(jìn)靶蛋白內(nèi)吞至溶酶體降解。然而,它們的降解效率和適用范圍受限于這些第三方溶酶體穿梭受體或E3連接酶的活性和表達(dá),而且強(qiáng)行“綁架”這些功能受體有可能導(dǎo)致潛在副作用。因此,開發(fā)一種不依賴第三方受體的細(xì)胞膜蛋白靶向降解技術(shù)至關(guān)重要。

文章上線截圖
1月9日,由中國(guó)科學(xué)院深圳先進(jìn)技術(shù)研究院(簡(jiǎn)稱“深圳先進(jìn)院”)醫(yī)藥所納米醫(yī)療技術(shù)研究中心李紅昌研究員、房麗晶研究員、蔡林濤研究員和邵喜明副研究員組成的學(xué)科交叉團(tuán)隊(duì),在國(guó)際知名期刊Nature Chemical Biology上以“Chemically Engineered Antibodies for Autophagy-based Receptor Degradation”為題發(fā)表最新研究成果。在這項(xiàng)研究中,他們成功開發(fā)出一種全新的基于自噬機(jī)制的細(xì)胞膜蛋白靶向降解技術(shù)——AUTAB(autophagy-inducing antibody)。該技術(shù)通過將細(xì)胞自噬誘導(dǎo)分子與細(xì)胞膜蛋白靶點(diǎn)抗體進(jìn)行共價(jià)偶聯(lián),實(shí)現(xiàn)了在不依賴額外細(xì)胞表面蛋白的情況下,精確觸發(fā)靶點(diǎn)蛋白通過自噬-溶酶體路徑降解。這一成果為以細(xì)胞膜蛋白為靶點(diǎn)的藥物研發(fā)提供了一種新的廣譜適用策略。
這項(xiàng)創(chuàng)新技術(shù)的靈感來源于,自然界中病原體感染和細(xì)胞膜損傷后細(xì)胞自主啟動(dòng)自噬進(jìn)行清除的現(xiàn)象。研究團(tuán)隊(duì)在篩選自噬誘導(dǎo)分子過程中發(fā)現(xiàn),有一種廣泛應(yīng)用于基因及藥物遞送的材料——聚乙烯亞胺(Polyethyleneimine,PEI),能夠高效誘導(dǎo)類似的細(xì)胞自噬。基于此發(fā)現(xiàn),團(tuán)隊(duì)利用點(diǎn)擊化學(xué)方法將PEI與能夠特異性識(shí)別目標(biāo)膜蛋白的抗體共價(jià)連接,成功構(gòu)建出一種既能精準(zhǔn)定位又能有效激活自噬機(jī)制的AUTAB分子,從而實(shí)現(xiàn)了對(duì)細(xì)胞膜蛋白的靶向降解。
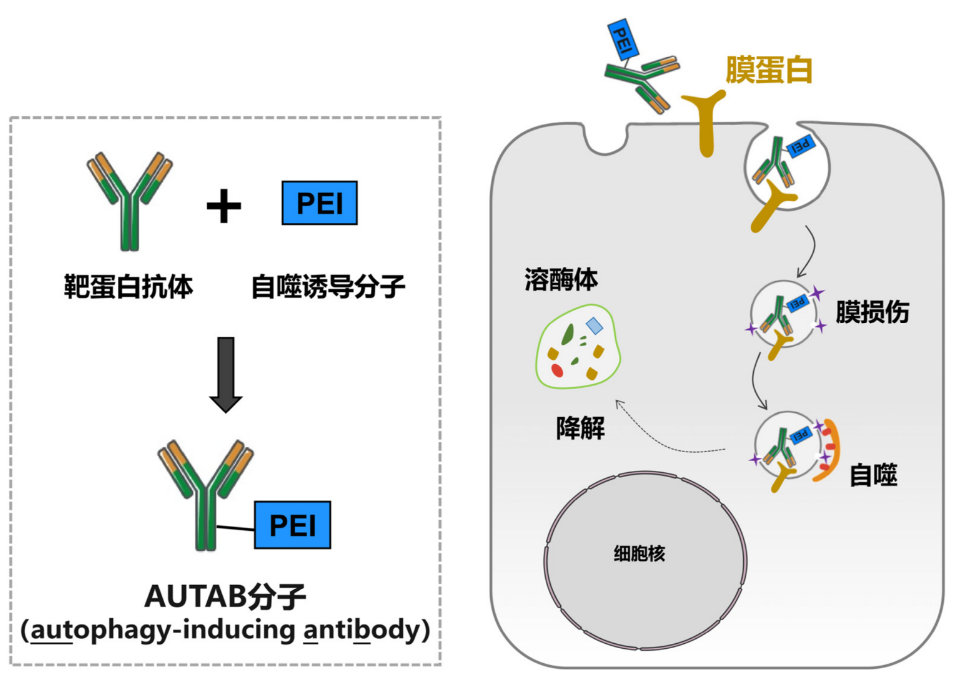
圖1. AUTAB分子的構(gòu)建原理和作用模式圖。
以腫瘤免疫治療靶點(diǎn)PD-L1為例,團(tuán)隊(duì)首先構(gòu)建了一種AUTAB分子進(jìn)行原理驗(yàn)證。深入研究表明,AUTAB通過抗體元件與靶點(diǎn)蛋白特異結(jié)合后,利用PEI元件造成靶點(diǎn)區(qū)域膜結(jié)構(gòu)微損傷,從而激活LC3C介導(dǎo)的自噬途徑,將靶點(diǎn)遞送至溶酶體降解。進(jìn)一步的生化結(jié)果也顯示,無論是通過溶酶體抑制劑抑制溶酶體功能,還是敲除自噬關(guān)鍵蛋白阻斷自噬發(fā)生,均能顯著干擾AUTAB的靶向降解活性,證實(shí)了AUTAB確實(shí)通過自噬-溶酶體路徑實(shí)現(xiàn)靶點(diǎn)降解。
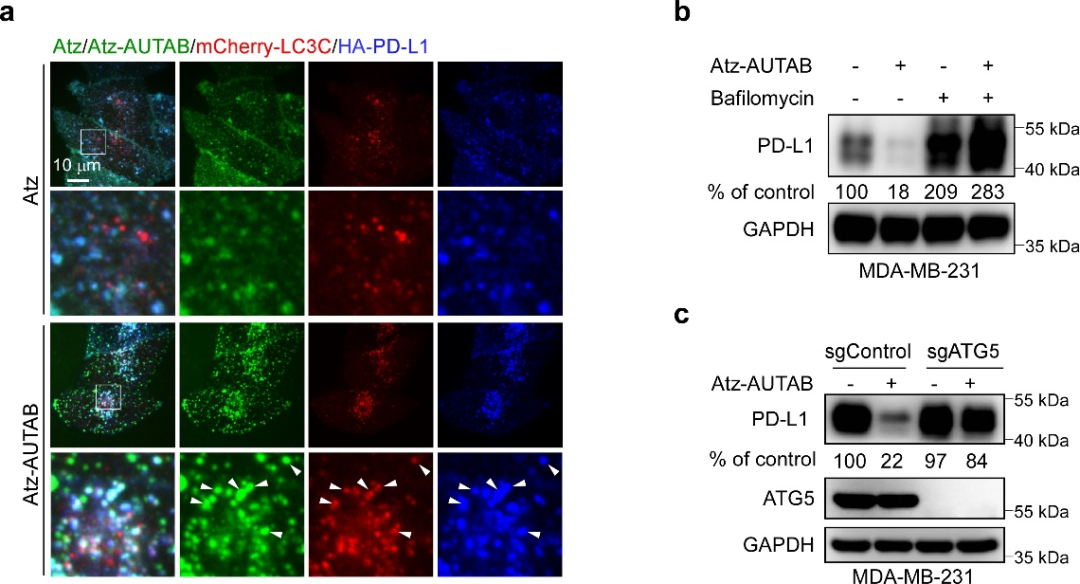
圖2. AUTAB技術(shù)的靶向蛋白自噬降解機(jī)制。(a) AUTAB誘導(dǎo)LC3C介導(dǎo)的自噬。(b) 溶酶體抑制劑Bafilomycin抑制AUTAB誘導(dǎo)的靶蛋白降解。(c) 敲除自噬關(guān)鍵蛋白ATG5抑制AUTAB誘導(dǎo)的靶蛋白降解。
在降解效率方面,由于細(xì)胞自噬本身就是一種將物質(zhì)高效定向遞送溶酶體機(jī)制,因此AUTAB分子僅需極低濃度(納摩爾)即可實(shí)現(xiàn)對(duì)靶蛋白的降解。更重要的是,團(tuán)隊(duì)驗(yàn)證了AUTAB技術(shù)的廣譜適用性:不僅在多種細(xì)胞類型中都可降解靶蛋白,而且針對(duì)包括膜錨定蛋白CD73在內(nèi)的各種膜蛋白均能實(shí)現(xiàn)高效靶向降解。
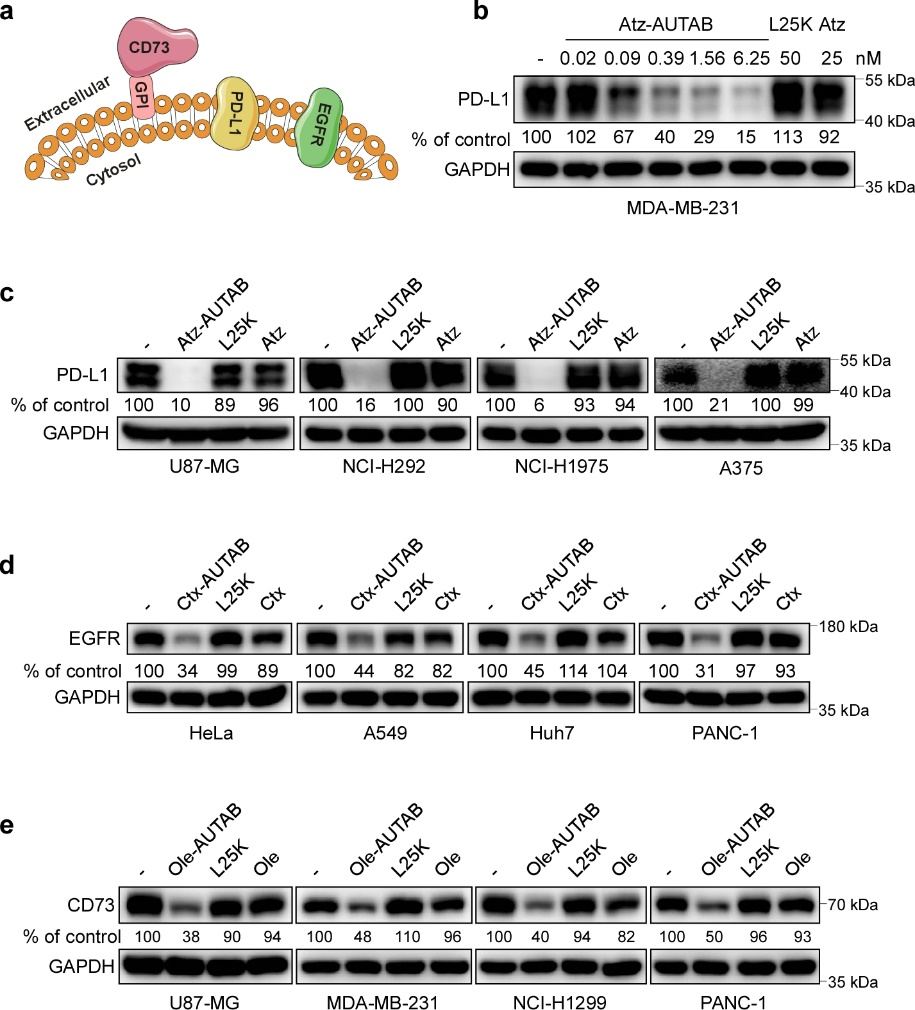
圖3. AUTAB技術(shù)的廣譜適用性。(a) 不同類型細(xì)胞膜蛋白的模式圖。(b) AUTAB誘導(dǎo)PD-L1降解的濃度效應(yīng)。(c-e) AUTAB在不同腫瘤細(xì)胞上誘導(dǎo)PD-L1,EGFR以及CD73降解效果的驗(yàn)證。
從化學(xué)機(jī)制角度,研究團(tuán)隊(duì)揭示了AUTAB分子中PEI攜帶的正電荷是誘導(dǎo)細(xì)胞膜蛋白降解的關(guān)鍵機(jī)制。利用化學(xué)修飾方法部分屏蔽PEI正電荷后,AUTAB分子降解細(xì)胞膜蛋白的效率明顯下降,而使用同樣帶正電荷的多聚賴氨酸可以完美替代PEI用于構(gòu)建AUTAB分子,這一結(jié)果從相反角度驗(yàn)證了AUTAB降解細(xì)胞膜蛋白的正電荷機(jī)制。
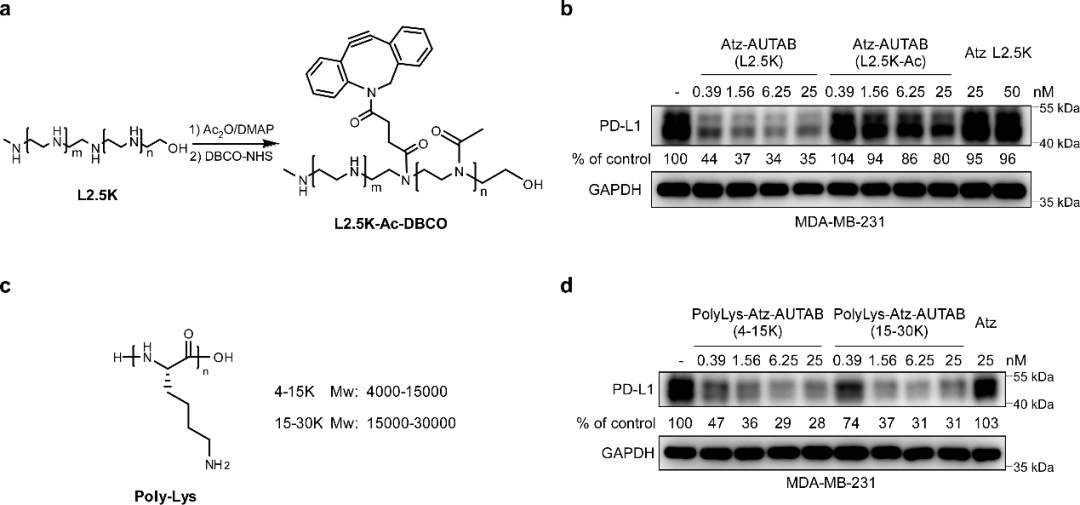
圖4. AUTAB技術(shù)的化學(xué)機(jī)制。?(a) 乙酰化封閉PEI正電荷。(b) 低電荷AUTAB誘導(dǎo)膜蛋白降解活性驗(yàn)證。(c) 攜帶正電荷的多聚賴氨酸化學(xué)結(jié)構(gòu)。(d) 多聚賴氨酸構(gòu)建的AUTAB分子誘導(dǎo)膜蛋白降解活性驗(yàn)證。
為提升AUTAB技術(shù)的使用可及性和便利性,研究團(tuán)隊(duì)進(jìn)一步開發(fā)了一種模塊化的Nano-AUTAB系統(tǒng)。不同于將PEI直接與靶點(diǎn)抗體偶聯(lián)形成AUTAB的技術(shù)路徑,Nano-AUTAB系統(tǒng)中的PEI被共價(jià)連接在一個(gè)能夠識(shí)別抗體IgG的納米二抗上,在使用時(shí)通過搭配不同的細(xì)胞膜蛋白抗體即可實(shí)現(xiàn)對(duì)各種細(xì)胞膜蛋白的靶向降解,由此獲得了一種通用AUTAB分子,展現(xiàn)出更加廣泛的應(yīng)用潛力。
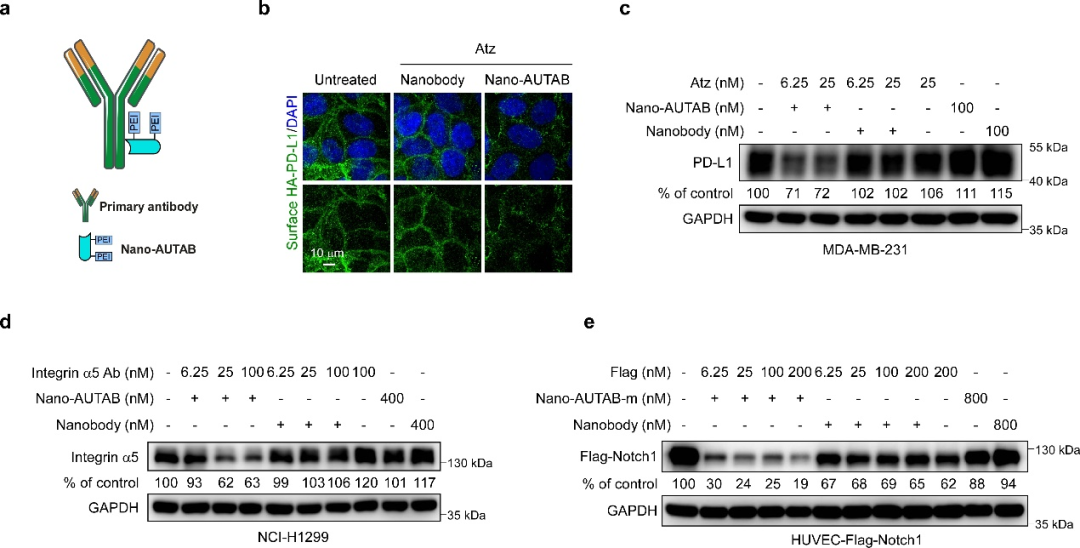
圖5. 模塊化的Nano-AUTAB。?(a) Nano-AUTAB模式圖。(b-c) Nano-AUTAB誘導(dǎo)PD-L1降解活性驗(yàn)證。(d) Nano-AUTAB誘導(dǎo)Integrin α5降解活性驗(yàn)證。(e) Nano-AUTAB誘導(dǎo)標(biāo)簽?zāi)J侥さ鞍捉到饣钚则?yàn)證。
綜上所述,該研究創(chuàng)新性地基于細(xì)胞自噬原理開發(fā)了一種細(xì)胞膜蛋白降解平臺(tái)。該技術(shù)不僅降解效率高,而且具有廣譜適用性和簡(jiǎn)單便捷性,未來無論在科學(xué)研究領(lǐng)域還是藥物研發(fā)方向,都具有重要應(yīng)用潛力。
深圳先進(jìn)院博士生程冰華、副研究員李梅青、研究助理鄭紀(jì)維是該論文的共同第一作者;李紅昌研究員、房麗晶研究員、蔡林濤研究員、邵喜明副研究員為論文共同通訊作者。該研究得到了國(guó)家重點(diǎn)研發(fā)計(jì)劃,國(guó)家自然科學(xué)基金,廣東省自然科學(xué)基金和深圳市科技計(jì)劃的資助。
團(tuán)隊(duì)專注于應(yīng)用交叉學(xué)科技術(shù),研發(fā)腫瘤等疾病的創(chuàng)新治療策略,相關(guān)成果發(fā)表在Nature Chemical Biology,Nature Nanotechnology等期刊。團(tuán)隊(duì)長(zhǎng)期招收化學(xué)生物學(xué),納米生物學(xué)和細(xì)胞生物學(xué)等相關(guān)專業(yè)的碩士/博士研究生和博士后,歡迎有志之士加入。
附件下載:


